I dette blogginnlegget skal jeg skrive om hydrokarboner. Hydrokarboner er organiske forbindelser som bare består av hydrogen- og karbonatomer. «Slike forbindelser finner vi enkelte sorter plast, propangass, parafin og skismøring og vaselin.»[1]
«Det er mulig å sette kjemiske navn på de ulike hydrokarbonene bare ved å se på strukturformelen. Den første delen av det kjemiske navnet bestemmes av hvor mange karbonatomer som befinner seg i rekke etter hverandre i molekylet. Det siste delen av navnet sier noe om bindingene i molekylet.»[2]
Navnsetting av hydrokarboner er som følger:
- Tell først antall karbon (C) i rekkefølge
| Antall karbonatomer i rekke |
Forstavelse
|
| 1 |
Met- |
| 2 |
Et- |
| 3 |
Prop- |
| 4 |
But- |
| 5 |
Pent- |
| 6 |
Heks- |
| 7 |
Hept- |
| 8 |
Okt- |
| 9 |
Non- |
| 20 |
Dek |
- Deretter ser du etter den største bindingen. Med andre ord betyr det at du skal se etter om det er en enkel elektronparbinding(alkaner), en dobbel elektronparbinding(alkener), eller en trippel elektronparbinding(alkyner).
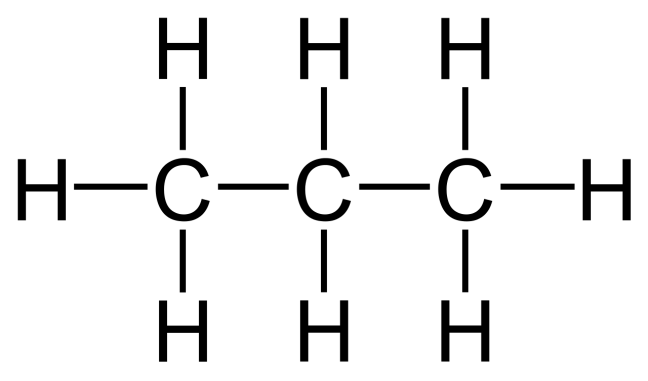
Kjemisk navn: Propan (3 C i rekke med enkeltbindinger)
Kjemisk formel: C(3) H(8)
Alkaner
Før vi går videre må vi gjøre rede for hva elektronparbindinger er og hvilke elektronparbindinger det er som finnes.
Hva er et mettet hydrokarbon?
Hydrogenatomet har plass til kun ett ekstra elektron i ytterste skall og kan derfor bare binde seg til ett annet atom med elektronparbinding. Karbonatomene har alltid fire armer, og regelmessig er det en arm som går til et karbonatom, mens de resterende blir fylt opp av hydrogenatomer. Når alle de ledige plassene som ikke er fylt med ett karbonatom (C), sier vi at molekylet er et mettet hydrokarbon.[3]
Hva er alkaner?
Alkanene er fellesnavnet for alle de mettede hydrokarbonene (der alle karbonatomer er bundet sammen med enkeltbindinger), men det finnes mange ulike alkaner. Alle alkaner har navn som slutter på -an. Alkaner har tidligere også vært kjent som parafin. Parafin som fås kjøpt i butikken er ingen kjemisk forbindelse, dessuten en blanding av ulike typer alkaner (hydrokarboner). [4]
Hvor finner vi alkaner?
På jorda vår finner det kun ørsmå mengder av det aller enkleste alkanet metan. Denne metanen stammer for det meste vulkaner, sumpområder, og tarmgassen fra drøvtyggere som kuer. Denne finnes også i menneskets tarm.[5]
Hvis du at kuene var noen miljøverstinger?
Når kua fordøyer gress får den hjelp av bakterier til å bryte ned denne maten. Vitenskapen vil ha det til at disse bakteriene samtidig som å fordøye også lager metan i store mengder. Forskning viser at en ku kan rape 500 liter metangass i døgnet. Som du sikkert har skjønt er utslippene så store at de har en påvirkning på klimaet, og metan er en gass som er drivhuseffekten i atmosfæren. Stadig vekk forskes det på fôr som er lettere å fordøye slik at kuene raper mindre, og at det får en mindre virkning på klimaet.
Alkener
Hva er et umettet hydrokarbon?
Tidligere har vi lært at karbonatomet har ledige armer som kan fylles av opptil fire andre atomer. Men det kan også bruke to eller tre av plassene på det samme karbonatomet, og da vil gå over fra å ha en enkelparbinding (alkan), til å enten ha en dobbeltparbinding eller en trippelparbinding (alkyn). Nå som disse armene er fylt opp med enten en dobbeltparbinding eller en trippelparbinding er det lenger ikke mye plass til mange hydrogenatomene som når det bare er enkeltbindinger. Slik definerer vi et umettet hydrokarbon.[6]
Alkenet eten – plantenes aldringshormon
Det enkleste alkenet er eten (også kalt etylen). Eten er den mest produserte organiske forbindelsen i verden og kan danne utgangspunkt for å lage mange andre kjemiske forbindelser, som polyetylen (plast). I naturen fungerer eten som et plantehormon, fordi det stimulerer modning av frukt og felling av blader. Under modningen skiller særlig epler og pærer ut mye eten. Det er derfor det ikke er lurt å la epler eller pærer ligge sammen med bananer, tomater eller annen frukt. Bananene kan da påvirkes av etenet fra eplene og raskere bli overmodne og brune. Etengassen fra et fruktfat vil også påvirke blomster, slik at de avblomstres raskere enn normalt.
Alkyner
Alkyner er umettede hydrokarboner med minst en trippelbinding i molekylet. Fordi trippelbindingen lett brytes, reagerer de raskt med andre stoffer. De kjemiske navnene til alkynene slutter alle på -yn. Det enkleste alkynet er er etyn, som består av to hydrogenatomer og to karbonatomer. Etyn kalles også for acetylen og brukes som sveisegass fordi den i blanding med oksygengass brenner med en svært varm flamme (over 3300 grader Celcius).[7]
«Karbidlamper ble tidligere brukt i gruver. De lyser ved at det drypper vann ned på kalsiumkarbidklumper i bunnen av lampen. Da dannes etyngass, som brenner og gir lys.»[8]
Hvorfor er det vanskelig å løse hydrokarboner i vann?
I Trigger 8 lærte vi at vannmolekylet er en dipol. Det vil si a det har en side som er elektrisk positiv, mens den andre er elektrisk negativ. I Hydrokarbonene trekker karbonatomene og hydrogenatomene omtrent like sterkt på elektronene(PH7), slik at den elektriske ladningen er jevnt fordelt. Derfor er ikke hydrokarbonmolekyler dipoler og ikke vannløselige.[9]
Hva er løsemidler?
Løsemidler er flytende væsker som brukes for å løse opp eller fortynne andre stoffer og holde dem i oppløst tilstand. De blir f.eks. brukt til å løse opp flekker på klær eller til å løse opp fargestoffene i maling og lakk. Når vi skal løse opp eller blande ut et stoff, må vi vite hva stoffet består av, for å være vannbasert og oljebasert (av hydrokarboner). Oljebasert maling vil derfor ikke løses i vann, men kan løses av andre hydrokarbonløsninger som f.eks. White spirit. Ioner/salter, sukker og mange andre stoffer er derimot polare og løses best i vann, siden vann i seg selv er en polar forbindelse. Huskeregelen når vi skal løse opp noe, er at «Likt løser likt». Med andre ord betyr det at vannbasert maling løses i vann.[10]
Hva bruker vi Hydrokarboner til?
Propan og butan brukes som brennstoff, for eksempel i gassbrennere og gassgriller. Heksan er en av flere komponenter du finner i bensin, men også i skokrem. Polyetylen en type plast, satt sammen av lange kjeder med etylen. I tillegg brukes parafinvoks i både skismøring og stearinlys.[11]
[1] Hydrokarboner, Trigger 10, s. 162.
[2] Faste regler, Trigger 10, s. 163.
[3] Alkaner, Trigger 10, s. 164
[4] Hva er alkaner? Trigger 10, s. 165
[5] Hvor finner vi alkaner? Trigger 10, s. 165
[6] Alkener, Hva er et umettet hydrokarbon? Trigger 10, s. 167
[7] Alkyner, Trigger 10, s. 168
[8] Oppsummering av navnsetting, Trigger 10, s. 170
[9] Hvorfor er det vanskelig å løse hydrokarboner i vann?1|2|q > Trigger 10, s. 167.
[10] Hva er løsemidler? Trigger 10, s. 171
[11] Hva bruker vi hydrokarboner til? Trigger 10, s. 172
– Zain